Naudojant cheminę energiją elektros energijai generuoti
2024-07-15
5102
Katalogas

1 paveikslas: Cheminė energija
Cheminės reakcijos proceso istorija
Elektros energijos generavimas per chemines reakcijas prasidėjo XVIII amžiuje, tai yra pagrindinis mokslinės istorijos etapas.Novatoriški Luigi Galvani tyrimai, paskelbti 1792 m., Sukūrė gilesnį supratimą apie bioelektrinius reiškinius.Galvani eksperimentai su varlių kojomis atskleidė, kad gyvūnų audiniai gali gaminti elektros sroves, kurias jis pavadino „gyvūnų elektra“.Remdamasis Galvani išvadomis, „Alessandro Volta“ sukūrė voltos krūvą 1800 m., Tai buvo pirmoji tikra baterija.Voltikinėse krūvoje buvo naudojami kintamieji sidabro ir cinko diskai, atskirti porėtos medžiagos, mirkytos sūraus vandens tirpale, sukuriant pastovią elektros srovę.Išsamios jo eksperimentų ir rezultatų, pateiktų Londono Karališkajai draugijai, dokumentavimas Volta paskatino išsamius elektros energijos pobūdžio ir galimo pritaikymo tyrimus.
Cheminės energijos apibrėžimas
Cheminė energija yra viena iš šešių pirminių energijos formų: elektrinė, spinduliuojanti, mechaninė, šiluminė ir branduolinė.Nors yra ir kitų formų, tokių kaip elektrocheminė, garso ir elektromagnetinė, cheminė energija daugiausia sujungia šias šešis.Šie sujungimai leidžia energijai gaminti įvairiais būdais.Idealiai tinka atlikti darbą, kuris moksliniu požiūriu reiškia jėgos pritaikymą objekto perkėlimui per atstumą.Cheminė energija išskiria energiją, kai reaguoja cheminės potencialo energija.Molekuliniame lygmenyje cheminė energija yra cheminių junginių jungtyse.Reakcijos metu šios molekulės sąveikauja, potencialiai sudarančios naujas medžiagas ir išleidžia energiją, kurią vėliau galima užfiksuoti ir panaudoti darbui.Pavyzdžiui, verdantis vanduo endoterminėje reakcijoje sugeria šilumą, paversdamas skystį garais.Ir atvirkščiai, kai garai sudaužo į skystį, jis išskiria šilumą egzoterminėje reakcijoje.Šis nuolatinis absorbcijos ir išsiskyrimo ciklas rodo pagrindinį cheminės energijos vaidmenį įvairiuose procesuose, nuo kasdienio iki nepaprasto.

2 paveikslas: endoterminė reakcija ir egzoterminė reakcija
Strenkdamas rungtynes, trintis sukuria pakankamai šilumos, kad galėtų pradėti cheminę reakciją rungtynių galvutės junginiuose.Ši reakcija išskiria energiją kaip šilumą ir šviesą, parodydama cheminės energijos virsmą tinkamu darbu.Mūsų kūne cheminė energija iš maisto virsta kinetine energija, skirta judėjimui ir šiluminei energijai kūno temperatūros palaikymui.Baterijos kaupia cheminę energiją, kuri paverčia elektrine energija į maitinimo įtaisus.Pavyzdžiui, išmaniojo telefono akumuliatoriuje yra cheminių junginių, kuriuose naudojama kontroliuojama reakcija, išleidžiant energiją, kuri maitina įrenginį.Šis procesas apima mikroskopines operacijas, siekiant užtikrinti nuoseklų ir patikimą energijos tiekimą.Cheminės energijos naudojimas apima šių reakcijų supratimą ir valdymą, siekiant optimizuoti efektyvumą ir saugumą.Pramoninėms reikmėms reikia tiksliai kontroliuoti temperatūros ir slėgio sąlygas, kad būtų maksimaliai padidinta energijos kiekis, tuo pačiu sumažinant riziką.Moksliniuose tyrimuose eksperimentuojant su skirtingais cheminiais junginiais, galima sukurti efektyvesnius energijos kaupimo sprendimus, pavyzdžiui, pažangias baterijas, turinčias didesnes pajėgumus ir greitesnį įkrovimo laiką.Norint parodyti didelę šios energijos formos poveikį mūsų pasauliui, reikalingas išsamus cheminių energijos procesų supratimas ir manipuliavimas cheminių energijos procesų supratimu ir kasdieninėmis galimybėmis.
Generuoti elektrą iš cheminių reakcijų
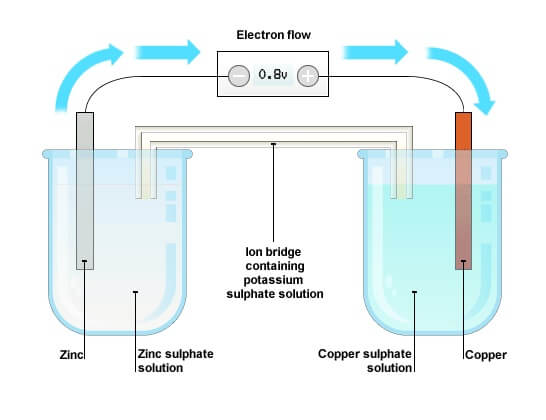
3 paveikslas: Cheminių reakcijų procedūra sukuria elektrą
Voltikinė krūva - kintami sidabro ir cinko diskai, atskirti porėta medžiaga, mirkoma druskingame vandenyje, parodo pagrindinius elektros energijos generavimo per chemines reakcijas principus.Sidabro gnybtas veikia kaip teigiamas elektrodas, o cinko gnybtas yra neigiamas elektrodas.„Volta“ patobulinimai naudojant vario ir cinko plokšteles lytiniame tirpale parodė, kaip skirtingos medžiagos gali padidinti efektyvumą.Cheminė ląstelė, pagrindinis elektros energijos gamybos vienetas, veikia palaikant beveik pastovią įtampą per du metalinius elektrodus, panardintus į rūgštinį ar šarminį tirpalą.Įprasta cheminė ląstelė gali naudoti vario ir cinko elektrodus Lye tirpale.Kelios ląstelės sudaro akumuliatorių, kuris tarnauja kaip tiesioginės srovės (DC) įtampos šaltinis, paverčiant cheminę energiją į elektrinę energiją.Konfigūracija - serija arba lygiagrečiai - nurodo bendrą įtampą ir srovę.Iš eilės atskiros ląstelių įtampos padidėja, o lygiagrečiai - srovės sujungia, palaikydamos pastovią įtampą.
Cheminės ląstelės veikimas prasideda nuo skirtingų metalų elektrodų panardinimo į elektrolitą (tai gali būti rūgšties, šarminės ar druskos tirpalas.) Elektrolitas yra idealus jonizacijos procesui, padalijimo atomams ir molekulėms į elektra įkrautos dalelės, vadinamos jonais, vadinamomis jonais,Sprendimo joninės pusiausvyros nustatymas.Kai cinko elektrodas yra panardintas į elektrolitą, jis iš dalies ištirpsta, gamindamas teigiamai įkrautus cinko jonus ir palikdamas laisvus elektronus ant elektrodo - sukuriant neigiamą krūvį.Vario elektrodas tame pačiame tirpale pritraukia teigiamus vandenilio jonus, juos neutralizuoja ir sudaro vandenilio dujų burbulus.Ši sąveika sukuria elektrinį potencialą tarp elektrodų.Potencialo dydis, apie 1,08 volto cinko-vamzdžio ląstelei, priklauso nuo naudojamų metalų.Šį potencialą palaiko nuolatinės cheminės reakcijos, kol sujungta apkrova, leidžianti elektronams tekėti iš neigiamo cinko elektrodo į teigiamą vario elektrodą.Galiausiai, generuojant elektros srovę.
Norint sukurti ir valdyti tokią cheminę ląstelę, reikia kruopščiai atkreipti dėmesį į detales.Operatorius turi užtikrinti metalinių diskų grynumą ir tinkamus matmenis, tiksliai paruošti elektrolito tirpalą ir atsargiai surinkti komponentus.Tai siekiama užkirsti kelią trumpiems jungimams ir maksimaliai padidinti efektyvumą.Pavyzdžiui, surenkant voltos krūvą, porėta medžiaga turi būti kruopščiai mirkoma sūraus vandens vandenyje, kad būtų išlaikytas nuolatinis laidumas tarp diskų.Norint užtikrinti saugų laidininkų ryšį kiekviename gale, norint stabiliam elektros išėjimui reikia sujungti.Šie principai apima įvairius šiuolaikinius įrenginius ir sistemas.Pavyzdžiui, surinkus elektroninių prietaisų baterijas, reikia kruopščiai suderinti ląsteles, išlaikyti optimalią elektrolitų koncentraciją ir užsitikrinti visas jungtis, kad patikimai veiktų.Pramoninėje aplinkoje tiksliai kontroliuojant temperatūros ir slėgio sąlygas cheminių ląstelių veikimo metu, idealiai tinka maksimaliai padidinti energijos kiekį ir užtikrinti saugumą.Šių subtilios veiklos detalių supratimas ir valdymas padidina cheminės energijos konvertavimo procesų efektyvumą ir patikimumą - pabrėžiant jų vaidmenį maitinant įvairias technologijas.
Cheminės energijos konvertavimas kasdienėje elektronikoje
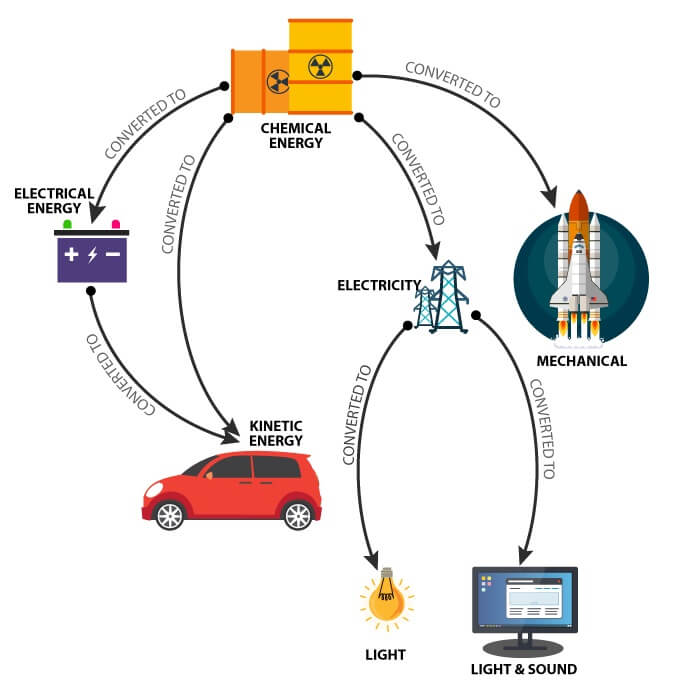
4 paveikslas: Cheminė energija, paverčiama kasdienine elektronika
Cheminės energijos konvertavimas į elektrinę energiją per ląsteles ir baterijas yra idealus į šiuolaikinę elektroniką.Ši technologija, atsirandanti nuo 1830 -ųjų telegrafo sistemų, padidino komercinių akumuliatorių gamybą, paverčiant ją pelninga pramone.Iki 1870 -ųjų baterijos varomi elektriniai varpai, o iki 1900 m. Žibintuvėlių gamyba kasmet pagamino daugiau nei du milijonus baterijų.Ši technologinė progresija tęsėsi, nes baterijos tapo pagrindine daugelio šiuolaikinių programų.Šiandien baterijos naudojamos daugelyje įrenginių ir sistemų.Akumuliatoriaus veikimas apima sudėtingus veiksmus, kurių kiekvienas reikalauja tikslumo ir supratimo.Pradėdamas vidinį degimo variklį, transporto priemonės akumuliatorius tiekia elektrinę energiją, kad galėtų maitinti starterio variklį ir uždegti variklį.Tam reikia, kad akumuliatorius išlaikytų stabilų krūvį, pasiektą tinkamai prižiūrint, pavyzdžiui, reguliariai tikrinant elektrolitų lygį ir švarias - saugias gnybtų jungtis, kad būtų išvengta korozijos ir užtikrintų efektyvų energijos perdavimą.
Baterijomis varomi šakiniai krautuvai yra plačiai naudojami ten, kur benzino variklio išmetimo dūmai kelia pavojų sveikatai.Šios baterijos turi būti reguliariai įkrautos ir tikrinamos dėl susidėvėjimo ar pažeidimo.Technikai laikosi išsamaus protokolo: įtampos lygio tikrinimo, elektrolitų koncentracijos tikrinimo ir įkrovimo įrangos užtikrinimo tinkamai.Šis kruopštus dėmesys užtikrina, kad šakiniai krautuvai išliks patikimi ir saugūs.Efektyvesnių elektrinių transporto priemonių (EV) baterijų kūrimas yra nemaža tyrimų sritis.Šioms baterijoms reikia pažangių medžiagų ir tikslios gamybos, kad būtų pasiektas didesnis energijos tankis ir ilgesnis gyvenimo trukmė.Tyrėjai ir inžinieriai stengiasi tobulinti katodo ir anodo medžiagas - optimizuoti elektrolitų sudėties ir pagerinti šiluminį valdymą, kad būtų išvengta perkaitimo ir padidintų akumuliatoriaus veikimo laiką.Nešiojamieji garso įrenginiai, pavyzdžiui, kompaktinių diskų grotuvai ir šiuolaikinė elektronika, pavyzdžiui, išmanieji telefonai ir nešiojamieji kompiuteriai, labai priklauso nuo baterijų.Šių įrenginių naudojimas apima akumuliatorių valdymo principų supratimą, kad būtų maksimaliai padidinta gyvenimo trukmė ir našumas.Pvz., Vartotojai turėtų vengti gilių iškrovimų ir vykdyti tinkamus įkrovimo ciklus, kad išlaikytų akumuliatoriaus sveikatą.Gamintojai naudoja akumuliatorių valdymo sistemas (BMS), norėdami stebėti ir valdyti įkrovos, temperatūros ir bendros akumuliatorių būklę.
Panašiai, baterijoms galia reikėjo funkcijų, esančių laikrodžiuose ir staliniuose kompiuteriuose - laiko ir atminties funkcijų palaikymas net tada, kai išjungta pagrindinė galia.Rašomuose laikrodžiuose akumuliatorius turi būti kompaktiškas, tačiau pakankamai galingas, kad ilgus metus tarnautų.Surinkimo procesas apima mažos baterijos įdėjimą į savo skyrių su tiksliais įrankiais, užtikrinant tinkamą kontaktą su vidine grandine, nepadarant žalos.Nešiojamųjų kompiuterių kompiuteriai gali visiškai veikti pagal akumuliatoriaus energiją, išryškindami pagrindinį cheminės energijos konvertavimo vaidmenį teikiant mobilumą.Nešiojamojo kompiuterio baterijų surinkimas apima ląstelių išdėstymą į kompaktišką ir efektyvią konfigūraciją.Šias baterijas dažnai stebi BMS, kad būtų galima subalansuoti įkrovimo ir išleidimo ciklus, kad būtų išvengta per didelio įkrovimo ir prailgintų akumuliatoriaus veikimo laiką.Vartotojai turėtų laikytis konkrečios įkrovimo praktikos, pavyzdžiui, išvengti visiško išleidimo ir nepalikti nešiojamojo kompiuterio, kuris nuolat prijungtas prie akumuliatoriaus efektyvumo.Baterijų raida ir pritaikymas pabrėžia transformacinį cheminės energijos konvertavimo poveikį kasdieninei elektronikai.Nuo ankstyvųjų telegrafo sistemų iki šių dienų modernių prietaisų, elektros energijos kaupimas ir išleidimas per chemines reakcijas skatina naujoves ir padidina daugybę technologijų funkcionalumo.
Cheminės energijos naudojimo poveikis aplinkai elektrai
Cheminės energijos panaudojimas elektros energijai gaminti, visų pirma per baterijas ir kuro elementus, turi didelį teigiamą ir neigiamą poveikį aplinkai.Norint priimti pagrįstus sprendimus dėl energijos gamybos ir naudojimo, būtina suprasti šį poveikį.
Teigiamas poveikis aplinkai.Vienas iš pagrindinių cheminės energijos (ypač baterijų pavidalo) naudojimo pranašumų yra šiltnamio efektą sukeliančių dujų išmetimo sumažėjimas, palyginti su tradiciniu iškastiniu kuru.Elektrinės transporto priemonės (EV), varomos iš ličio jonų baterijų, sukuria nulinį išmetimo vamzdžio išmetimą, nepaprastai sumažindamos oro taršą ir prisideda prie švaresnės miesto aplinkos.Panašiai atsinaujinančios energijos kaupimo sistemos, naudojančios chemines baterijas, gali laikyti ir išsiųsti elektrą iš atsinaujinančių šaltinių, tokių kaip saulės ir vėjas.Įgalinant nuoseklesnį ir patikimesnį atsinaujinančios energijos tiekimą.
Neigiamas poveikis aplinkai.Nepaisant šių privalumų, yra keletas aplinkosaugos problemų, susijusių su cheminių baterijų gamyba, naudojimu ir šalinimu.Žaliavų, tokių kaip ličio, kobaltas ir nikelis, ištraukimas, idealiai tinka gaminti akumuliatorių, gali sukelti didelį aplinkos degradaciją.Kasybos operacijos dažnai lemia buveinių sunaikinimą, vandens taršą ir padidėjusį anglies išmetimą.Be to, šios medžiagos yra baigtinės, o jų ekstrahavimas ne visada yra tvarus.Taip pat pats baterijų gamybos procesas yra daug energijos reikalaujantis ir gali sukelti didelę išmetimą bei atliekas.Gamyklos, gaminančios baterijas, sunaudoja daug energijos, dažnai gaunamos iš neatsinaujinančių šaltinių, todėl padidėja anglies pėdsakas.Be to, gamybos procesas apima pavojingas chemines medžiagas, jei jis nėra tinkamai valdomas, gali sukelti aplinkos užteršimą.
Išleidimo ir perdirbimo iššūkiai.Baterijų išvežimo pabaigos pabaiga yra dar vienas reikšmingas aplinkos apsaugos iššūkis.Baterijose yra toksiškų medžiagų, tokių kaip švinas, kadmis ir rūgštys.Tai gali išplauti į dirvožemį ir vandenį, jei jie nebus tinkamai išmesti.Dėl netinkamo sąvartynų baterijų šalinimo gali būti užteršta aplinka ir kelti pavojų žmonių sveikatai.Baterijų perdirbimas yra didžiulis žingsnis sušvelninant šį neigiamą poveikį.Tačiau perdirbimo procesas yra sudėtingas ir nėra visuotinai įgyvendinamas.Nors perdirbimas gali atkurti vertingas medžiagas ir sumažinti naujų žaliavų ištraukimo poreikį, ji dažnai yra brangi ir techniškai sudėtinga.Daugeliui regionų trūksta tinkamos perdirbimo infrastruktūros, dėl kurių maža perdirbimo norma ir nuolatinė žala aplinkai dėl netinkamo akumuliatoriaus šalinimo.
Švelninantis poveikis aplinkai.Dedamos pastangos sušvelninti cheminės energijos naudojimo poveikį aplinkai elektrai.Akumuliatorių technologijos naujoves siekiama sumažinti priklausomybę nuo retų ir toksiškų medžiagų, padidinti energijos tankį ir pagerinti perdirbimą.Pavyzdžiui, tyrėjai tiria alternatyvas, tokias kaip kietojo kūno baterijos ir ličio sieros baterijos, kurios žada didesnį efektyvumą ir mažesnį poveikį aplinkai.Vyriausybės ir pramonės vadovai stengiasi sukurti efektyvesnius perdirbimo metodus ir įgyvendinti taisykles, skatinančias tinkamą baterijų šalinimą ir perdirbimą.Visuomenės sąmoningumo kampanijos taip pat gali vaidinti vaidmenį ugdant vartotojus apie akumuliatorių perdirbimo svarbą.
Išvada
Apibendrinant galima pasakyti, kad cheminės energijos konvertavimas nepaprastai suformavo technologinę aplinką - nuo ankstyvų dienų su Galvani ir Volta iki šiuolaikinių pritaikymų kasdienėje elektronikoje.Įvaldę cheminių reakcijų principus ir kruopščiai valdydami sudėtingus susijusius procesus, mes sukūrėme patikimus energijos kaupimo sprendimus, tokius kaip baterijos, kurios maitina daugybę prietaisų.Ši kelionė pabrėžia transformacinę cheminės energijos galią skatinant naujoves, gerinant funkcionalumą ir patenkinti šiuolaikinės visuomenės energijos poreikius.Taikant tyrimus ir toliau verčiant efektyvumo ir pajėgumų ribas, cheminės energijos konvertavimo ateitis žada dar didesnį pažangą.Būkite tikri, kad ši energijos forma išlieka nuostabi technologinei pažangai ir kasdieniam gyvenimui.
Dažnai užduodami klausimai [DUK]
1. Kaip baterijos cheminę energiją paverčia elektrine energija?
Baterijos paverčia cheminę energiją į elektrinę energiją per elektrochemines reakcijas.Akumuliatoriaus viduje yra du elektrodai: anodas ir katodas, atskirtas elektrolitu.Kai akumuliatorius prijungtas prie prietaiso, tarp anodo ir elektrolito įvyksta cheminė reakcija, išleidžiant elektronus.Šie elektronai teka per išorinę grandinę į katodą, sukuriant elektros srovę, kuri maitina prietaisą.Elektrolitas palengvina jonų judėjimą akumuliatoriuje, kad subalansuotų elektronų srautą.Šis procesas tęsiasi tol, kol reagentai išeikvojami, tada akumuliatorių reikia įkrauti arba pakeisti.
2. Ar efektyvus cheminės energijos konvertavimo į elektrinę energiją procesas?
Cheminės energijos konvertavimo į elektrinę energiją efektyvumas baterijose skiriasi, tačiau paprastai svyruoja nuo 70% iki 90%.Tai reiškia, kad nuo 70% iki 90% cheminės energijos paverčiama elektrine energija, o likusi dalis prarandama kaip šiluma.Veiksniai, darantys įtaką efektyvumui, yra akumuliatoriaus rūšis, naudojamos medžiagos ir eksploatavimo sąlygos.Pavyzdžiui, ličio jonų akumuliatoriai yra žinomi dėl savo efektyvumo ir yra plačiai naudojami vartojimo elektronikoje ir elektrinėse transporto priemonėse.Tačiau visos baterijos patiria tam tikrą energijos praradimą dėl vidinio pasipriešinimo ir kitų veiksnių, o tai šiek tiek sumažina jų bendrą efektyvumą.
3. Kuo skiriasi cheminė energija akumuliatoriuose ir kuro elementuose?
Tiek baterijos, tiek kuro elementai cheminę energiją paverčia elektrine energija, tačiau jos veikia skirtingai.Baterijos kaupia cheminę energiją savo ląstelėse ir išleidžia ją per vidines reakcijas.Tai yra savarankiškos sistemos, kurias kelis kartus galima įkrauti ir pakartotinai naudoti.Kita vertus, kuro elementai nuolat konvertuoja cheminę energiją iš išorinio kuro šaltinio (pavyzdžiui, vandenilio) į elektrą.Jie reikalauja nuolatinio degalų ir deguonies tiekimo, kad būtų galima generuoti galią.Nors baterijos yra tinkamos nešiojamoms ir mažesnio masto programoms, kuro elementai dažnai naudojami didesnio masto ir nuolatinėms galios poreikiams, pavyzdžiui, transporto priemonėse ir nejudančioje energijos gamyboje.
4. Kokie yra cheminės energijos naudojimo kaip elektrinės energijos šaltinio naudojimo apribojimai?
Cheminės energijos naudojimas kaip elektrinės energijos šaltinis turi keletą apribojimų.Pirma, akumuliatorių talpa yra baigtinė, tai reiškia, kad jas reikia įkrauti arba pakeisti, kai tik išeikvota.Tai gali būti nepatogu programoms, reikalaujančioms ilgalaikės galios.Antra, baterijų gamyba ir šalinimas gali sukelti aplinkos iššūkių dėl toksiškų medžiagų naudojimo ir taršos galimybių.Be to, baterijos turi ribotą gyvenimo trukmę, kuriai dažnai reikia pakeisti po tam tikro skaičiaus įkrovos ciklų.Temperatūros jautrumas yra dar viena problema;Ekstremali temperatūra gali paveikti akumuliatoriaus našumą ir gyvenimo trukmę.Galiausiai, nors daroma pažanga, akumuliatorių energijos tankis ir akumuliatorių saugojimo galimybės vis dar atsilieka nuo kitų formų energijos kaupimo, pavyzdžiui, iškastinio kuro.
5. Kiek laiko įtaisai gali galioti naudojant cheminę energiją, prieš tai, kai reikia įkrovimo ar pakeitimo?
Trukmė, kurią įtaisai, varomi iš cheminės energijos, gali trukti prieš tai, kai reikia papildymo ar pakeitimo, priklauso nuo kelių veiksnių, įskaitant akumuliatoriaus tipą, įrenginio energijos suvartojimą ir akumuliatoriaus talpą.Pvz., Išmanusis telefonas su ličio jonų akumuliatoriumi gali trukti visą dieną vienu įkrovimu su įprastu naudojimu, o išmanusis laikrodis gali trukti kelias dienas.Didesni prietaisai, kaip ir elektrinės transporto priemonės, gali nuvažiuoti šimtus mylių vienu įkrovimu.Tačiau senstant baterijoms, jų pajėgumas mažėja, todėl sutrumpėja laikas tarp krūvių.Įkraunamų baterijų gyvenimo trukmė paprastai yra nuo kelių šimtų iki kelių tūkstančių įkrovimo ciklų, kol jų našumas žymiai pablogina, todėl reikia pakeisti.
 APIE MUS
Klientų pasitenkinimas kiekvieną kartą.Abipusis pasitikėjimas ir bendrieji interesai.
APIE MUS
Klientų pasitenkinimas kiekvieną kartą.Abipusis pasitikėjimas ir bendrieji interesai.
Funkcijos testas.Aukščiausi ekonomiškai efektyvūs produktai ir geriausia paslauga yra mūsų amžinas įsipareigojimas.
Karštas straipsnis
- Yra CR2032 ir CR2016 keičiami
- MOSFET: apibrėžimas, darbo principas ir atranka
- Relės montavimas ir bandymai, relės laidų diagramų aiškinimas
- CR2016 ir CR2032 Koks skirtumas
- NPN ir PNP: Koks skirtumas?
- ESP32 vs STM32: Kuris mikrovaldiklis jums yra geresnis?
- LM358 Dvigubo eksploatavimo stiprintuvo išsamus vadovas: „Pinouts“, grandinės schemos, ekvivalentai, naudingi pavyzdžiai
- CR2032 VS DL2032 VS CR2025 palyginimo vadovas
- Suprasti skirtumus ESP32 ir ESP32-S3 Techninės ir veiklos analizė
- Išsami RC serijos grandinės analizė
 Naršymas įtampos reguliatorių pasirinkimas: išsamus vadovas
Naršymas įtampos reguliatorių pasirinkimas: išsamus vadovas
2024-07-15
 L293d vs L298N: skirtumas tarp L293D ir L298N
L293d vs L298N: skirtumas tarp L293D ir L298N
2024-07-12
Karštos dalies numeris
 C1608NP02A2R2C080AA
C1608NP02A2R2C080AA CC1206JRNPO0BN180
CC1206JRNPO0BN180 06036A391KAT2A
06036A391KAT2A LD031A330JAB4A
LD031A330JAB4A GRM1886R1H101JZ01D
GRM1886R1H101JZ01D TAJS685M010RNJ
TAJS685M010RNJ M85049/38-13W
M85049/38-13W PM200DV1A120
PM200DV1A120 8V97051NLGI
8V97051NLGI ATF22V10C-10JC
ATF22V10C-10JC
- VI-JT0-EZ
- VS-60EPS08-M3
- M29W040B90N1
- ATUC256L3U-AUT
- RT1206DRD07140RL
- RT1206DRD07110RL
- SKM400GAL128DE
- VI-J03-10
- AM4377BZDNA80
- TIG052TS-TL-E
- ADXL357BEZ-RL7
- TPS65145PWPR
- LP3982IMM-3.3/NOPB
- HMC576LC3BTR
- J201
- T495D157M006ATE065
- XC2VP20-6FFG896C
- XC2VP7-5FF896C
- AS7C4098-15TI
- EPC2TC32U
- FFPF30UP20DP
- HD6433837UC67X
- LTC1382CS
- N80C196KB
- SRM2B256SL-TMX70
- TMS320DM642GNZ
- TPS54320RHL
- VSP2200Y
- MIC4428YMTR
- A3S12D30ETP-G5
- K4D623238B-QC55
- K6F8016R6B-EF70
- W39L040AP-70B
- TMS27PC512-15FML
- VSC7391HO
- L2D2295-Q9CPCGFAA
- V48C5C500AL
- STM32H7A3RGT6
- UPD78062GF